ヒンデンブルグ号の悲劇という事件をご存じですか?
1937年5月ドイツのヒンデンブルグ号という飛行船がアメリカで爆発炎上した事件です。
飛行船
飛行船というのは、大きな気球のようなものです。
全盛期には大西洋を越えて就航していました。
飛行船は浮かぶために、気球内部に軽いガスを詰めています。

内部に詰めるガスには水素やヘリウムが考えられます。
水素は可燃性ですがヘリウムガスは不活性ガスであり、燃えることがありません。
現代ではアドバルーンのような気球にはヘリウムガスが使用されています。
しかし、ヒンデンブルグ号はガスに可燃性の水素を使用していたのです。
ヒンデンブルグ号の悲劇
ヒンデンブルグ号はドイツから大西洋を横断飛行してアメリカへ到着したのですが、着陸の際火災を起こし、結果的に爆発炎上してしまいます。
そして、乗員・乗客97人中35人と地上の作業員1名が死亡したという記録が残っています。

ヒンデンブルグ号の爆発の原因はいろいろ推測されているようですが、外皮塗装に使われていた材料が静電気により発火したとされる説が有力です。
しかし、気球の中身が可燃性の水素なので火災が起これば当然、爆発炎上の危険は高まります。
では、中身のガスを水素から燃えないヘリウムに代えればいいのではないか?誰しも考えることです。
ここで水素とヘリウムについて考えてみましょう。
水素 $H_2$、ヘリウム $He$ で示されます。
分子量はだいたい次の値です。
$H_2$ $He$ 2 4 これを見ると、ヘリウムは水素の約2倍の質量をもつことになります。
問題
次の疑問が浮かびます。
気球内のガスをすべてヘリウムにすると水素の2倍の重さになるから、飛行船が運べる重量は半分になる。
そのため、運べる重量が激減する。
ところが実際には、ガスを水素からヘリウムに変えたからと言ってその飛行能力にはほとんど違いは出ないのです。つまり運搬できる重量はほとんど同じだったのです。
さて、問題です。
飛行船の中身のガスを水素からヘリウムに変えても、なぜその運搬能力にほとんど違いが出なかったのでしょうか?
答えを見る前に・・・ちょっと考えてみましょう。
解答
動画
確かにモル数が同じであれば、ヘリウムは同温同圧同体積で水素の2倍の質量をもちます。
では具体的に計算してみましょう。
例えば、$224000\:\mathrm{L}$ の体積がある気球にガスを詰めます。
浮力はその物体の重さには無関係であり、その体積だけに関係します。
このとき気球の持つ浮力はその気球に空気を詰めた場合の、その空気の重さに等しくなります。
これを計算してみましょう。

理想気体では、0℃ 1気圧 1 $\mathrm{mol}$ で 22.4 L を占めます。
ここでは簡単のためこの条件を使います。
今、気球体積が、$224000\:\mathrm{L}$ ですから $\dfrac{224000}{22.4}=10000 \:\mathrm{mol} $ です。またモルの定義から、モル数 $n$、気体質量 $m$、分子量が $M$ とすると、
$n=\dfrac{m}{M}$
つまり、$m=n\times M$ となります。
空気は混合気体なので、平均的な分子量を考えてだいたい、28.8 です。したがって、「空気の重さ=気球にかかる浮力の大きさ」は、
$m=n\times M=10000 \times 28.8 =288 \:\mathrm{kg} $ ほどです。
よって、浮力の大きさは、$288\:\mathrm{kg}$ になります。実際に持ち上げられる重量はここから気球自体の重さと中に詰められたガスの重さを引く必要があります。
では中身に気球に水素を詰めた場合の、水素ガスの質量を具体的に計算してみましょう。
水素では $M_{H_2}=2$ だったので、
$m=10000\times 2=20000 \:g=20\:\mathrm{kg}$ です。
つまり、この水素気球に詰められた水素ガスの重さは具体的にはだいたい $20\:\mathrm{kg}$ です。
次に、水素をヘリウムに置き換えてみましょう。
長々と計算せずとも、ヘリウムの $M_{He}=4$ つまり水素の倍なので、気球に詰められたヘリウムガスの質量はだいたい $40\:\mathrm{kg}$ です。
水素とヘリウムの差は $40-20 =20 \:\mathrm{kg}$ ですので、水素のほうが約 $20\:\mathrm{kg}$ 分だけ多く持ち上げることができる計算になります。
しかし、浮力は $288\:\mathrm{kg}$ だったわけですから、それほど浮揚能力に違いはありません。
ましてや、飛行船の浮揚能力が半分になるということはありません。
つまり、気球内部のガスを水素からヘリウムに置き換えたところで、中のガスの重さが2倍になるだけです。そして、水素もヘリウムもとても軽い気体なので、全体にはそれほど影響はない・・・ということですね。
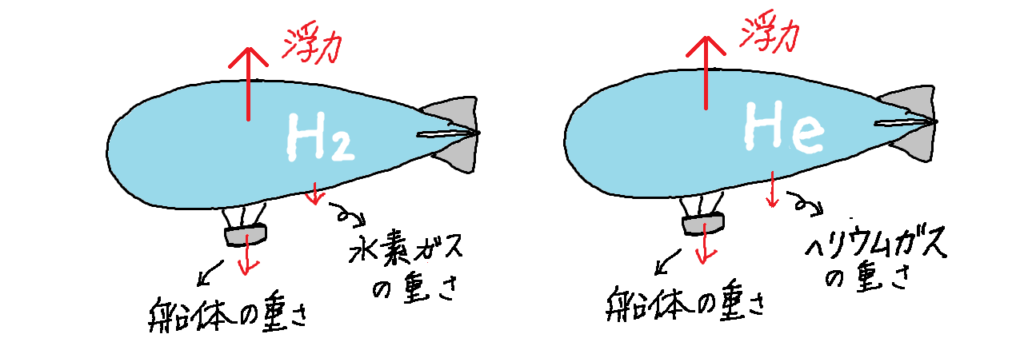
ガスの種類で浮力は変わらない!
加えて、ガスはそもそも軽いので
たとえガスの重さが2倍になっても影響は少ない!というわけですね。



コメント