熱効率
熱効率は記号 $e$ で示される物理量です。
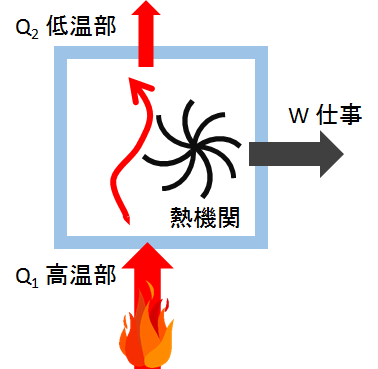
熱機関が、高温部(熱源)から熱 $Q_1$ を吸収し、$W$ の仕事を行い、低温部へ $Q_2$ の熱を捨てるとします。
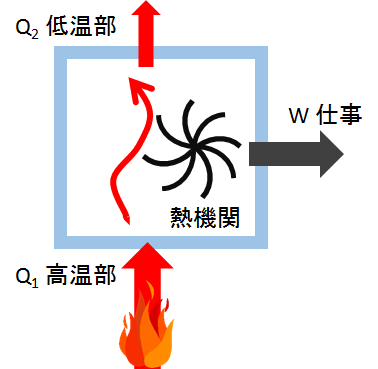

そうすると、熱エネルギーを、有効に仕事に変換できた率を熱効率 $e$ として、次の式で定義されます。
$熱効率=\dfrac{仕事}{吸収した熱量}$
$e=\dfrac{W}{Q_1}$
です。

たとえて言えば、お小遣いを 1000 円 もらったとしましょう。
そして、お菓子を 600 円 買いました。
しかし、痛恨!お菓子屋へ行く途中で 400 円 落としてしまいました。
有効に使えた割合は、$\frac{お菓子の代金}{お小遣い}$ です。
この割合が熱効率と同じ考え方です。
ここで、$Q_1$ と $Q_2$ および $W$ の関係ですが、エネルギーが保存されますから、 図からもわかるように $Q_1=W+Q_2$ です。
これより、 $W=Q_1-Q_2$ となりますから、
$e=\dfrac{W}{Q_1}$
$e=\dfrac{Q_1-Q_2}{Q_1}$
です。
ここで熱力学第2法則から、捨てる熱 $Q_2$ は $0$ になることはありません。
したがって、必ず $0\leqq e<1$ です。
いろいろな熱機関の熱効率を示します。
ガソリンエンジン 0.2 ~ 0.3
ディーゼルエンジン 0.3 ~ 0.4
思ったより低いと思いませんか?
ガソリンエンジンでガソリンの2割から3割程度しか、車の運動エネルギーになっていません。
変換できなかった残りはどうなったのでしょうか?
それは、普通の熱機関では外部に熱として捨てられていたのです。
驚きですね。

効率低いですね。
さらに、たとえば $ 40\:L$ のガソリンを燃やして自動車でドライブしたとします。結局、最後は自宅に帰って車を車庫へ入れるわけですから、すべてのガソリンの持っていたエネルギーは熱として環境に放出されるということになります。
・・・これじゃあ温暖化するわな。














コメント